Forum
Warto wiedzieć
Twoje Forum
Forum Giełda
+Dodaj wątek
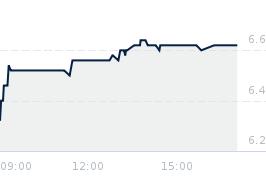
Opublikowano przy kursie:
6,78 zł
, zmiana od tamtej pory:
-50,00%
Pytanie dla dociekliwych akcjonariuszy ; )
Zgłoś do moderatoraPharmena poinformowała nas o podpisaniu umów na dystrybucję produktów na rynkach USA, Kanady i Meksyku z przychodnia lekarską w Colorado. przychodnia ta ponoć wyprzedała na pniu partię Endoteliol.
każdy z nas wie, że aby wprowadzić produkt spożywczy lub medyczny na rynek USA, potrzebna jest zgoda FDA.
pytanie dla dociekliwych (m.in. wuja i mistrza):
dlaczego Pharmena nie opublikowała komunikatu jak zrobiło to MedApp w dniu 28.06.2022?
Tytuł: Złożenie zgłoszenia produktu CarnaLife Holo do Agencji Żywności i Leków w Stanach Zjednoczonych (U.S. Food and Drug Administration, FDA)
"Zarząd Spółki MedApp S.A. z siedzibą w Krakowie („Spółka”) niniejszym informuje, że w dniu 28.06.2022 r. Spółka za pośrednictwem firmy Parexel International, w ramach procesu 510 (k) wysłała do Agencji Żywności i Leków USA [Food and Drug Administration (FDA)] wniosek o potwierdzenie zgodności umożliwiające wprowadzenie produktu CarnaLife Holo jako wyrobu medycznego klasy II na rynek USA. Potwierdzenie zgodności przez FDA będzie oznaczać możliwość wprowadzenia CarnaLife Holo do szpitali i klinik na rynku USA, jako produktu wspomagającego i pogłębiającego diagnostykę pacjentów w kontekście planowania zabiegów medycznych.
Pozytywna opinia FDA dla danego produktu zwyczajowo uznawana jest także poza terytorium USA jako wyznacznik jakości i potwierdzenie braku negatywnego wpływu na zdrowie."
czyżby nie było się czym chwalić? czy jest inny powód?
każdy z nas wie, że aby wprowadzić produkt spożywczy lub medyczny na rynek USA, potrzebna jest zgoda FDA.
pytanie dla dociekliwych (m.in. wuja i mistrza):
dlaczego Pharmena nie opublikowała komunikatu jak zrobiło to MedApp w dniu 28.06.2022?
Tytuł: Złożenie zgłoszenia produktu CarnaLife Holo do Agencji Żywności i Leków w Stanach Zjednoczonych (U.S. Food and Drug Administration, FDA)
"Zarząd Spółki MedApp S.A. z siedzibą w Krakowie („Spółka”) niniejszym informuje, że w dniu 28.06.2022 r. Spółka za pośrednictwem firmy Parexel International, w ramach procesu 510 (k) wysłała do Agencji Żywności i Leków USA [Food and Drug Administration (FDA)] wniosek o potwierdzenie zgodności umożliwiające wprowadzenie produktu CarnaLife Holo jako wyrobu medycznego klasy II na rynek USA. Potwierdzenie zgodności przez FDA będzie oznaczać możliwość wprowadzenia CarnaLife Holo do szpitali i klinik na rynku USA, jako produktu wspomagającego i pogłębiającego diagnostykę pacjentów w kontekście planowania zabiegów medycznych.
Pozytywna opinia FDA dla danego produktu zwyczajowo uznawana jest także poza terytorium USA jako wyznacznik jakości i potwierdzenie braku negatywnego wpływu na zdrowie."
czyżby nie było się czym chwalić? czy jest inny powód?
- Pytanie dla dociekliwych akcjonariuszy ; )
- Re: Pytanie dla dociekliwych akcjonariuszy ; )
- Re: Pytanie dla dociekliwych akcjonariuszy
- Re: Pytanie dla dociekliwych akcjonariuszy
- Re: Pytanie dla dociekliwych akcjonariuszy
- Re: Pytanie dla dociekliwych akcjonariuszy
- Re: Pytanie dla dociekliwych akcjonariuszy
- Kurs Euro
- Kurs dolar
- Kurs frank
- Kurs funt
- Wiron
- Przelicznik walut
- Kantor internetowy
- Kalkulator wynagrodzeń
- Umowa zlecenie
- Kredyt na mieszkanie
- Kredyt na samochód
- Kalkulator kredytowy
- Revolut
- Winiety
- Jak grać na giełdzie?
- Jak wziąć kredyt hipoteczny?
- Rejestracja samochodu
- Jak rozwiązać umowę z Orange
- Koszty uzyskania przychodów
- Sesje elixir
- PB weekend
- RRSO co to jest?
- Blogbank.pl
- Promocje bankowe
- Stopa procentowa