Forum
Warto wiedzieć
Twoje Forum
Forum Giełda
+Dodaj wątek
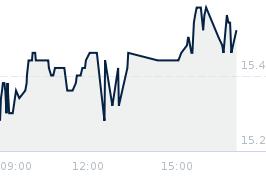
Opublikowano przy kursie:
30,70 zł
, zmiana od tamtej pory:
-30,78%
info
Zgłoś do moderatoraRozwinięcie informacji zawartej w RB 5/2020 dotyczącego rozwoju i wdrożenia wysokowydajnego
testu qRT-PCR do diagnostyki zakażeń SARS-COV-2
W dniu 13 marca 2020 roku, podjęto decyzję o priorytetowym zaadoptowaniu strefy BSL-3 i wdrożeniu
wytwarzania testów do diagnostyki qRT-PCR w nowopowstających laboratoriach spółki w Kazuniu Nowym, tzw.
Centrum Badawczo Rozwojowym.
Centrum Badawczo Rozwojowe Spółki zostało zaprojektowane jako zintegrowane środowisko, w
którym przewidziano możliwości przeprowadzania diagnostyki molekularnej, w tym w klasie BCSL-3 dla potrzeb
naszych zaplanowanych projektów onkologicznych i immunomodulacyjnych.
Zakres adaptacji pod potrzeby diagnostyki SARS-COV-2 oceniamy jako minimalny do
zaimplementowania i zgodny z dotychczasowymi projektami. Niezbędna aparatura jest w trakcie realizacji
finasowanie zabezpieczone w ramach już przyznanych Spółce projektów. Inwestycja spółki z własnych środków
nie powinna przekroczyć kwoty 0,5-1 mln zł.
Opracowywany test, dla którego uzyskano pierwszą pozytywną ocenę analiz retrospektywnych, operaty
jest na ultraszybkiej technologii one-step qRT-PCR. Technologia ta polega na 1- stopniowej amplifikacji
specyficznej sekwencji DNA wirusa bezpośrednio na matrycy próbki biologicznej.
Tego typu testy są zgodne z najnowszą rekomendowaną przez WHO metodą szybkich i wiarygodnych
badań skriningowych na SARS-COV-2. Zdaniem Spółki wynik diagnostyczny wg. testu powinien być uzyskiwany
w czasie 12-24 h. Wynik będzie dostępny drogą elektroniczną, co skróci czas oczekiwania na informację.
Spółka będzie przygotowywać dwutorową metodę komercjalizacji:
1) Sprzedaż testu do instytucji (ew. zasobów bezpieczeństwa zdrowia publicznego)
2) Wykonywania testów usługowo na użytek zdrowotnych instytucji publicznych i prywatnych.
Spółka przewiduje moce wytwórcze w ramach CBR w zakresie komercjalizacji i sprzedaży testów na
poziomie od kilkudziesięciu do kilkuset tysięcy sztuk kwartalnie.
W zakresie komercjalizacji usługowej, przewiduje się możliwość wykonywania do 300 testów dziennie,
przy założeniu dwuzmianowej pracy.
Spółka zdecydowała się na implementacje samodzielnej produkcji elementów testu ze względu na
posiadane zasoby, doświadczenie oraz infrastrukturę nowopowstałego CBR. Tego typu podejście pozwoli na
uniezależnienie się od zewnętrznych źródeł podobnych testów.
Zarząd Spółki oczekuje pełnej gotowości w zakresie masowego wytwarzania i sprzedaży testów przed
sezonem jesiennym, a także gotowości do wykonywania badań w tym okresie.
dr Maciej Wieczorek, Prezes Zarządu Celon Pharma S.A.
testu qRT-PCR do diagnostyki zakażeń SARS-COV-2
W dniu 13 marca 2020 roku, podjęto decyzję o priorytetowym zaadoptowaniu strefy BSL-3 i wdrożeniu
wytwarzania testów do diagnostyki qRT-PCR w nowopowstających laboratoriach spółki w Kazuniu Nowym, tzw.
Centrum Badawczo Rozwojowym.
Centrum Badawczo Rozwojowe Spółki zostało zaprojektowane jako zintegrowane środowisko, w
którym przewidziano możliwości przeprowadzania diagnostyki molekularnej, w tym w klasie BCSL-3 dla potrzeb
naszych zaplanowanych projektów onkologicznych i immunomodulacyjnych.
Zakres adaptacji pod potrzeby diagnostyki SARS-COV-2 oceniamy jako minimalny do
zaimplementowania i zgodny z dotychczasowymi projektami. Niezbędna aparatura jest w trakcie realizacji
finasowanie zabezpieczone w ramach już przyznanych Spółce projektów. Inwestycja spółki z własnych środków
nie powinna przekroczyć kwoty 0,5-1 mln zł.
Opracowywany test, dla którego uzyskano pierwszą pozytywną ocenę analiz retrospektywnych, operaty
jest na ultraszybkiej technologii one-step qRT-PCR. Technologia ta polega na 1- stopniowej amplifikacji
specyficznej sekwencji DNA wirusa bezpośrednio na matrycy próbki biologicznej.
Tego typu testy są zgodne z najnowszą rekomendowaną przez WHO metodą szybkich i wiarygodnych
badań skriningowych na SARS-COV-2. Zdaniem Spółki wynik diagnostyczny wg. testu powinien być uzyskiwany
w czasie 12-24 h. Wynik będzie dostępny drogą elektroniczną, co skróci czas oczekiwania na informację.
Spółka będzie przygotowywać dwutorową metodę komercjalizacji:
1) Sprzedaż testu do instytucji (ew. zasobów bezpieczeństwa zdrowia publicznego)
2) Wykonywania testów usługowo na użytek zdrowotnych instytucji publicznych i prywatnych.
Spółka przewiduje moce wytwórcze w ramach CBR w zakresie komercjalizacji i sprzedaży testów na
poziomie od kilkudziesięciu do kilkuset tysięcy sztuk kwartalnie.
W zakresie komercjalizacji usługowej, przewiduje się możliwość wykonywania do 300 testów dziennie,
przy założeniu dwuzmianowej pracy.
Spółka zdecydowała się na implementacje samodzielnej produkcji elementów testu ze względu na
posiadane zasoby, doświadczenie oraz infrastrukturę nowopowstałego CBR. Tego typu podejście pozwoli na
uniezależnienie się od zewnętrznych źródeł podobnych testów.
Zarząd Spółki oczekuje pełnej gotowości w zakresie masowego wytwarzania i sprzedaży testów przed
sezonem jesiennym, a także gotowości do wykonywania badań w tym okresie.
dr Maciej Wieczorek, Prezes Zarządu Celon Pharma S.A.
- Kurs Euro
- Kurs dolar
- Kurs frank
- Kurs funt
- Wiron
- Przelicznik walut
- Kantor internetowy
- Kalkulator wynagrodzeń
- Umowa zlecenie
- Kredyt na mieszkanie
- Kredyt na samochód
- Kalkulator kredytowy
- Revolut
- Winiety
- Jak grać na giełdzie?
- Jak wziąć kredyt hipoteczny?
- Rejestracja samochodu
- Jak rozwiązać umowę z Orange
- Koszty uzyskania przychodów
- Sesje elixir
- PB weekend
- RRSO co to jest?
- Blogbank.pl
- Promocje bankowe
- Stopa procentowa